PERKEMBANGAN TEORI ATOM
a. Teori atom Dalton
Menurut Dalton atom adalah bagian terkecil dari suatu materi yang tidak dapat dibagi lagi. Namun ternyata pendapat ini tidak benar karena ditemukannya partikel-partikel dasar elektron, proton dan neutron.
Model Atom Dalton

b. Teori Atom Thomson
Menurut Thomson bentuk atom menyerupai agar-agar tersusun dari muatan listrik positif dan negatif. Muatan positif menyebar secara merata dalam bulatan yang merupakan atom dan elektron terdapat di dalamnya.
Model Atom Thomson

c. Model Atom Rutherford
Atom adalah bola berongga yang tersusun dari inti atom dan elektron yang mengelilinginya. Inti atom bermuatan positif dan massa atom terpusat pada inti atom. Kelemahan dari Rutherford tidak dapat menjelaskan mengapa elektron tidak jatuh ke dalam inti atom. Berdasarkan teori fisika, gerakan elektron mengitari inti ini disertai pemancaran energi sehingga lamakelamaan energi elektron akan berkurang dan lintasannya makin lama akan mendekati inti dan jatuh ke dalam inti.
Model Atom Rutherford
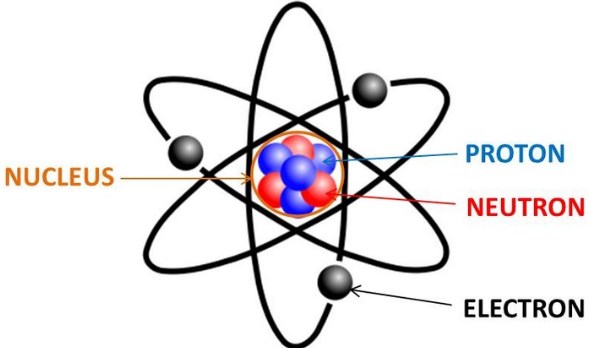
d. Model Atom Niels Bohr
– Atom terdiri atas inti yang bermuatan positif dan dikelilingi oleh elektron yang bermuatan negatif di dalam suatu lintasan.
– Elektron dapat berpindah dari satu lintasan ke yang lain dengan menyerap atau memancarkan energi sehingga energi elektron atom itu tidak akan berkurang. Jika berpindah lintasan ke lintasan yang lebih tinggi, elektron akan menyerap energi. Jika beralih ke lintasan yang lebih rendah, elektron akan memancarkan energi.
– Kedudukan elektron-elektron pada tingkat-tingkat energi tertentu yang disebut kulit-kulit elektron.
Model Atom Bohr

e. Model Atom Modern
Kulit-kulit elektron bukan kedudukan yang pasti dari suatu elektron, tetapi hanyalah suatu kebolehjadian saja.
Model Atom Modern
